BAB II Revisi
description
Transcript of BAB II Revisi
BAB II
TINJAUAN PUSTAKA
2.1 Tanaman Manggis (Garcinia mangostana L.)
2.1.1 Klasifikasi Tanaman Manggis (Garcinia mangostana L.)
Divisi : Spermatophyta
Sub divisi : Angiospermae
Kelas : Dicotyledoneae
Bangsa : Parietales
Suku : Guttiferae (Clusiaceae)
Marga : Garcinia
Jenis : Garcinia mangostana L. (Depkes RI, 1994)
2.1.2 Deskripsi Tanaman Manggis (Garcinia mangostana L.)
Pohon manggis memiliki tinggi kurang lebih 15 meter. Batang berkayu, bulat,
tegak, percabangan simpodial, berwarna hijau kotor. Daun tunggal, lonjong, ujung
runcing, pangkal tumpul, tepi rata, pertulangan menyirip, panjang 20-25 cm, lebar
6-9 cm, tebal, tangkai silindris, berwarna hijau. Bunga tunggal, berkelamin dua,
tumbuh di ketiak daun, tangkai silindris, panjang 1-2 cm, benang sari berwarna
kuning, memiliki satu putik berwarna putih. Buah berbentuk bulat, diameter 6-8
cm, warna coklat keunguan. Biji berbentuk bulat, diameter kurang lebih 2 cm,
dalam satu buah terdapat 5-7 biji, berwarna kuning. Akar tunggang, berwarna
putih kecoklatan (Depkes RI, 1994).
5
6
Gambar dari tanaman manggis (Garcinia mangostana L.) dapat dilihat pada
gambar 2.1 di bawah ini.
Gambar 2.1. Tanaman manggis (Garcinia mangostana L.)
2.1.3 Kandungan Kimia Tanaman Manggis (Garcinia mangostana L.)
Akar dan kulit batang manggis mengandung saponin, flavonoid, dan polifenol.
Kulit buah manggis mengandung saponin, antosianin, dan tanin (Depkes RI,
1994; Supiyanti dkk., 2010). Menurut Jung et al. (2006), xanton yang terkandung
dalam kulit buah manggis yaitu cudraxanthone G, 8-deoxygartanin,
garcimangosone B, garcinone D, garcinone E, gartanin, 1-isomangostin, α-
mangostin, γ-mangostin, mangostinone, smeathxantone A , dan tovophyllin A.
Metabolit sekunder utama dari tanaman ini yaitu α-mangostin, β-mangostin, dan
γ-mangostin (Chin et al, 2008).
2.1.4 Khasiat dan Bioaktivitas Tanaman Manggis (Garcinia mangostana L.)
Berdasarkan usada, kulit buah manggis digunakan untuk mengobati sakit bibir
(Putra, 1991). Ekstrak kulit buah manggis memiliki aktivitas sebagai antioksidan,
7
antikanker, anti-inflamasi, antialergi, antibakteri, antifungi, antivirus, serta
antimalaria (Chaverri et al., 2008). Isolat α-mangostin dari kulit buah manggis
juga telah terbukti memiliki aktivitas sebagai antidislipidemia (Dachriyanus dkk.,
2007).
2.2 Hewan Uji
Hewan uji yang umumnya digunakan dalam penelitian yaitu tikus putih
(Rattus norvegicus L). Keuntungan penggunaan tikus putih dalam percobaan yaitu
mudah dipelihara, relatif sehat, cocok untuk berbagai macam penelitian,
mempunyai kemiripan dengan manusia dalam hal fisiologi, anatomi, nutrisi,
patologi, metabolisme serta umum digunakan untuk penelitian mengenai kadar
lipid darah. Penggunaan tikus putih jantan dalam percobaan bertujuan untuk
mengurangi pengaruh perubahan hormonal, dimana tikus jantan memiliki sedikit
hormon estrogen sehingga tidak mempengaruhi kadar lipid darahnya. Tikus galur
Wistar mempunyai kepala yang besar dengan ekor yang lebih pendek dan dapat
mencapai ukuran 40 cm yang diukur dari hidung sampai ujung ekor dengan berat
berkisar antara 140-500 gram (Harini dan Astirin, 2009; Manurung dkk., 2012;
Suwandi, 2012).
2.3 Lipid
Lipid merupakan suatu senyawa yang bersifat hidrofobik yang terdapat dalam
semua bagian tubuh serta dapat diekstraksi dari mahluk hidup. Lipid tidak larut
dalam air dan dapat diangkut ke dalam peredaran darah dengan mengikat protein
8
yang larut dalam air (Murray et al., 2003). Lipid plasma yang utama yaitu
kolesterol, trigliserida dan fosfolipid (Ganiswarna dkk., 2004).
2.3.1 Kolesterol
Kolesterol berfungsi untuk regulasi cairan tubuh; unsur dari myelin dalam
jaringan saraf; bahan baku untuk penyusun beberapa jenis biomolekul seperti
hormon steroid, asam empedu, dan vitamin D (Boyer, 2002). Kolesterol berasal
dari dua sumber yaitu, dari makanan (eksogen) dan kolesterol endogen yang
disintesis oleh tubuh. Apabila jumlah kolesterol dari makanan berkurang maka
sintesis kolesterol di dalam hati dan usus akan meningkat untuk memenuhi
kebutuhan jaringan dan organ lainnya. Kolesterol yang diproduksi dalam hati
dibantu dengan enzim yang disebut HMG-KoA reduktase, kemudian kolesterol
dikirimkan ke dalam aliran darah (Linn et al., 2009).
2.3.2 Trigliserida
Trigliserida disintesis dari asam-asam lemak dan gliserol, proses pembentukan
tersebut dikenal sebagai proses lipogenesis (deposisi lemak). Proses pemecahan
trigliserida menjadi gliserol dan asam lemak oleh enzim lipase serta melepasnya
ke dalam pembuluh darah disebut dengan proses lipolisis (mobilisasi lemak)
(Guyton, 1995; AHA, 2006).
2.3.3 Fosfolipid
Jenis fosfolipid yang utama yaitu lesitin, sefalin, dan sfingomielin. Fosfolipid
sebagian besar dibentuk dalam sel hati (Guyton, 1995). Fosfolipid adalah unsur
pokok dari membran sel, dimana strukturnya mirip dengan trigliserida. Pada
bagian kepala molekul terdapat nitrogen yang bersifat hidrofilik. Pada bagian
9
ujung ekor terdapat asam lemak yaitu asam lemak jenuh dan tak jenuh yang
bersifat hidrofobik (Sloane, 2004).
2.3.4 Lipoprotein
Lipid plasma dimodifikasi dalam bentuk kompleks makromolekul agar dapat
ditransportasikan dalam sirkulasi. Modifikasi tersebut dilakukan dalam bentuk
lipoprotein. Lipoprotein plasma terdiri atas sebagian besar fosfolipid, kolesterol
bebas dan protein, sedangkan pada intinya tersusun oleh sebagian besar
trigliserida dan kolesterol ester (Ganiswarna dkk., 2004, Dipiro et al., 2005).
Struktur lipoprotein dapat dilihat pada gambar 2.2.
Gambar 2.2 Struktur Lipoporotein Plasma (Burns et al., 2008)
Lipoprotein dibedakan menjadi 5 golongan besar, yaitu :
a. Kilomikron
Kilomikron terdiri dari 80% trigliserida yang berasal dari makanan dan
kurang dari 5% kolesterol ester. Kilomikron membawa trigliserida dari
makanan ke jaringan lemak dan otot rangka dan membawa kolesterol dari
makanan ke hati (Ganiswarna dkk., 2004).
10
b. Lipoprotein densitas sangat rendah (VLDL, very low density lipoprotein)
VLDL terdiri dari 60% trigliserida dan 10-15% kolesterol. VLDL
berfungsi mengangkut lipid yang disintesis di hati menuju ke seluruh tubuh
(Ganiswarna dkk., 2004).
c. Lipoprotein densitas sedang (IDL, intermediet density lipoprotein).
IDL adalah zat perantara yang terjadi saat VLDL dikatabolisme menjadi
LDL. IDL terdiri atas 30% trigliserida, 20% kolesterol dan relatif lebih
banyak mengandung apolipoprotein B dan E (Ganiswarna dkk., 2004).
d. Lipoprotein densitas rendah (LDL, low density lipoprotein).
LDL merupakan metabolit VLDL yang berfungsi mengangkut kolesterol
ke jaringan perifer untuk sintesis membran plasma dan hormon steroid. LDL
terdiri atas 10% trigliserida dan 50% kolesterol (Ganiswarna dkk., 2004).
e. Lipoprotein densitas tinggi (HDL, high density lipoprotein).
HDL terdiri atas 13% kolesterol, kurang dari 5% trigliserida, dan 50%
protein. HDL berfungsi mengangkut kolesterol dari jaringan perifer ke hati
sehingga penimbunan kolesterol di perifer berkurang (Ganiswarna dkk.,
2004).
2.4 Metabolisme Lipid
Lipid darah diangkut dengan 2 cara yaitu jalur eksogen dan jalur endogen.
1. Jalur Eksogen
Kolesterol dan asam lemak bebas yang masuk ke dalam tubuh melalui usus
akan diserap di mikrovili usus, selanjutnya akan diubah menjadi kolesterol ester
11
dan trigliserida. Trigliserida dan kolesterol ester tersebut akan dikemas sebagai
kilomikron. Kilomikron akan diangkut dalam saluran limfe lalu dibawa ke dalam
darah. Di dalam kapiler jaringan lemak dan otot, trigliserida dalam kilomikron
mengalami hidrolisis oleh lipoprotein lipase yang terdapat pada permukaan sel
endotel. Akibat hidrolisis ini maka akan terbentuk asam lemak dan kilomikron
remnan. Asam lemak bebas akan menembus endotel dan masuk ke dalam jaringan
lemak atau sel otot untuk diubah menjadi trigliserida kembali atau dioksidasi.
Kilomikron remnan ini akan dibersihkan oleh hati dari sirkulasi dengan
mekanisme endositosis dan lisosom. Hasil metabolisme ini berupa kolesterol
bebas yang akan digunakan untuk sintesis berbagai struktur membran plasma,
myelin, hormon steroid dan lain sebagainya, serta disimpan dalam hati sebagai
kolesterol ester lagi atau diekskresi ke dalam empedu sebagai kolesterol atau asam
empedu atau diubah menjadi lipoprotein endogen yang dikeluarkan ke dalam
plasma. Kolesterol juga dapat disintesis dari asetat dibawah pengaruh enzim
HMG-KoA reduktase yang menjadi aktif jika terdapat kekurangan kolesterol
endogen. Asupan kolesterol dari darah juga diatur oleh jumlah reseptor LDL yang
terdapat pada permukaan sel hati (Ganiswarna dkk., 2004).
2. Jalur Endogen
Pada jalur endogen, trigliserida dan kolesterol yang disintesis oleh hati
diangkut secara endogen dalam bentuk VLDL. VLDL yang banyak mengandung
trigliserida akan dihidrolisis oleh lipoprotein lipase dalam sirkulasi. VLDL
kemudian dimetabolisme oleh enzim lipase menjadi partikel lipoprotein yang
lebih kecil yaitu IDL. IDL kemudian berubah menjadi LDL. Apabila katabolisme
12
LDL oleh hati dan jaringan perifer berkurang, maka kadar kolesterol plasma akan
meningkat (Ganiswarna dkk., 2004; Fauci et al, 2008).
2.5 Dislipidemia Pada Tikus
Dislipidemia adalah gangguan metabolisme lipid yang ditandai dengan
peningkatan salah satu atau lebih kadar lipid yang meliputi kadar kolesterol total,
Low-Density Lipoprotein (LDL), dan trigliserida maupun penurunan kadar High-
Density Lipoprotein (HDL) dalam darah (Wells et al., 2006; Linn et al., 2009).
Penyebab kerusakan primer pada dislipidemia adalah ketidakmampuan
pengikatan LDL pada reseptor LDL atau kerusakan dalam proses pencernaan
kompleks LDL kedalam sel setelah pengikatan normal. Hal ini mengarah pada
kurangnya degradasi LDL oleh sel dan tidak teraturnya biosintesis kolesterol.
Dengan kurangnya reseptor LDL maka jumlah kolesterol total dan LDL menjadi
tidak seimbang (Sukandar dkk., 2008; Linn et al., 2009; Subramaniam et al,
2011). Klasifikasi kolesterol total, LDL, HDL, dan trigliserida pada tikus dapat
dilihat pada table 2.1.
Tabel 2.1. Klasifikasi kolesterol total, LDL, HDL, dan trigliserida pada tikus
Lipid Darah Keterangan
Kolesterol Total- 10-54 mg/dL Normal
LDL - 17-22 mg/dL Normal
HDL- 77-84 mg/dL Normal
Trigliserida- 26-145 mg/dL Normal
(Ratnayanti, 2011)
13
2.6 Simvastatin
Simvastatin merupakan salah satu obat golongan statin yang digunakan untuk
terapi dislipidemia. Obat ini menghambat kerja enzim HMG-KoA reduktase
menjadi asam mevalonat sehingga sintesis kolesterol dalam hati berkurang. Hal
ini mengakibatkan jumlah reseptor LDL meningkat. LDL akan lebih banyak
masuk ke dalam hati untuk yang kemudian diekskresikan melalui empedu.
Simvastatin mampu menurunkan kadar LDL, kadar trigliserida, kadar kolesterol
total dan meningkatkan kadar HDL (Ganiswarna dkk., 2004).
2.7 Metode Induksi Dislipidemia
Timbulnya dislipidemia pada hewan coba dapat dilakukan dengan
memberikan makanan yang dapat meningkatkan kadar kolesterol. Penilaian
terjadinya dislipidemia dapat dilakukan dengan mengukur kadar kolesterol total,
HDL, LDL dan trigliserida pada hewan uji.
Berdasarkan penelitian yang dilakukan oleh Nugroho et al. (2012), induksi
makanan diet lemak tinggi dengan 15% lemak babi, 5% kuning telur bebek
selama 55 hari berhasil merangsang peningkatan kadar kolesterol, trigliserida, dan
LDL pada darah tikus. Lemak babi memiliki kadar lemak yang lebih tinggi
daripada kadar lemak pada sapi. Kadar asam lemak jenuh ganda pada babi juga
lebih besar daripada sapi (Hermanto dkk., 2008).
Mekanisme peningkatan kadar kolesterol berasal dari trigliserida yang masuk
dari makanan diemulsikan oleh asam empedu, kemudian diserap oleh usus halus.
Di dalam pankreas terdapat dua enzim yaitu enzim lipase dan enzim fosfolipase
14
A2. Enzim lipase menghidrolisis trigliserida menjadi 1,2-digliserida dan 2-
gliserida, sedangkan enzim fosfolipase A2 menghidrolisis fosfolipid menjadi asam
lemak dan lisofosfolipid. Semua produk tersebut ditransportasikan ke sel epitel
usus, di tempat ini trigliserida disintesis kembali. Trigliserida bersama protein,
fosfolipid, dan kolesterol ester bergabung membentuk kilomikron. Trigliserida
yang terdapat dalam kilomikron ini akan dihidrolisis oleh enzim lipoprotein lipase
menjadi asam lemak dan gliserol. Asam lemak akan memasuki sel-sel jaringan,
sebagian akan diubah menjadi energi dan sebagian lagi akan dioksidasi menjadi
asetil-KoA yang merupakan prekusor pembentuk kolesterol (Dachriyanus dkk.,
2007).
Pemberian diet kuning telur dapat menaikkan kadar profil lipid, terutama
kadar kolesterol total dan trigliserida. Pemberian diet kuning telur pada tikus
sangat mempengaruhi metabolisme kadar kolesterol darah. Diet kuning telur yang
kaya kolesterol dan trigliserida diuraikan oleh enzim lipase lambung yang
sebelumnya diemulsikan oleh garam empedu. Hasil penguraiannya berupa asam
lemak bebas dan dua monogliserida dalam bentuk misel dalam usus halus. Asam
lemak bebas dan monogliserida disintesis kembali oleh epitel usus halus menjadi
trigliserida dan fosfolipid, kemudian bergabung dengan kilomikron, diangkut
menuju hati dan jaringan (Prasetyo dkk., 2000).
2.8 Etanol
Etanol merupakan pelarut organik yang umunya digunakan dalam proses
ekstraksi. Etanol dapat meningkatkan permeabilitas dinding sel simplisia sehingga
15
proses ekstraksi menjadi lebih efisien dalam menarik komponen polar hingga
semi polar. Etanol 95% terdiri atas 95% etanol dan 5% air. Etanol memiliki titik
didih pada suhu 78,40C dan titik beku pada suhu -1120C. Etanol dapat larut dalam
air dan eter, mudah terbakar, tidak berwarna, tidak berasa, serta memiliki bau
yang khas (Siedel, 2008).
2.9 Ekstrak
Ekstrak merupakan sediaan kering, kental atau cair yang diperoleh dengan
cara menyari simplisia nabati atau hewani menurut cara yang cocok, diluar
pengaruh cahaya matahari langsung (Depkes RI, 1979). Penyarian ekstrak
menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut
diuapkan dan massa atau serbuk yang tersisa diperlakukan sedemikian rupa
hingga memenuhi baku yang telah ditetapkan (Depkes RI, 2000).
2.10 Metode Ekstraksi
Penyarian adalah kegiatan penarikan zat yang dapat larut dari bahan yang
tidak dapat larut dengan pelarut cair, sehingga zat aktif akan berada dalam cairan
pelarut tersebut. Faktor yang mempengaruhi kecepatan penyarian adalah adalah
kecepatan difusi zat yang larut melalui lapisan-lapisan batas antara cairan panyari
dengan bahan yang mengandung zat tersebut. Maserasi merupakan teknik
penyarian yang sederhana dan digunakan untuk penyarian simplisia yang
mengandung zat aktif yang mudah larut dalam cairan penyari, tidak mengandung
16
zat yang mudah mengembang dalam cairan penyari, tidak mengandung benzoin,
stirak, dan lain-lain (Depkes RI, 1986; Kristanti et al., 2008).
Cairan penyari yang digunakan dapat berupa air, etanol, air-etanol, atau
pelarut lain. Maserasi dilakukan dengan merendam serbuk simplisia dalam cairan
penyari. Cairan penyari akan menembus dinding sel dan masuk ke dalam rongga
sel yang mengandung zat aktif, zat aktif akan larut pada cairan penyari dan karena
adanya perbedan konsentrasi antara larutan zat aktif di dalam sel dengan yang di
luar sel, maka larutan yang terpekat didesak keluar. Peristiwa tersebut terjadi
berulang sehingga terjadi keseimbangan konsentrasi antara larutan di luar sel
dengan larutan di dalam sel (Depkes RI, 1986).
Pada umumnya maserasi dapat dilakukan dengan cara: 10 bagian simplisia
dengan derajat halus yang cocok dimasukkan ke dalam bejana, kemudian dituangi
dengan 75 bagian cairan penyari, ditutup dan dibiarkan selama 5 hari terlindung
dari cahaya, sambil berulang-ulang diaduk. Setelah 5 hari sari diserkai, ampas
diperas. Ampas ditambah cairan penyari secukupnya diaduk dan diserkai,
sehingga diperoleh seluruh sari sebanyak 100 bagian. Benjana ditutup, dibiarkan
ditempat sejuk, terlindung dari cahaya, selama 2 hari. Kemudian endapan
dipisahkan (Depkes RI, 1986).
Keuntungan cara penyarian dengan maserasi adalah cara pengerjaan dan
peralatan yang digunakan sederhana dan mudah diusahakan. Sedangkan kerugian
cara maserasi adalah pengerjaannya lama dan penyariannya kurang sempurna,
cairan penyari yang digunakan lebih banyak serta tidak dapat digunakan untuk
bahan-bahan yang mempunyai tekstur keras seperti benzoin, tiraks dan lilin. Pada
17
penyarian dengan cara maserasi, perlu dilakukan pengadukan. Pengadukan ini
diperlukan untuk meratakan konsentrasi larutan di luar butir serbuk simplisia,
sehingga dengan pengadukan, dapat tetap terjaga derajat perbedaan konsentrasi
yang sekecil-kecilnya antara larutan di dalam sel dengan larutan di luar sel. Hasil
penyarian dengan cara maserasi perlu dibiarkan selama waktu tertentu. Waktu
tersebut diperlukan untuk mengendapkan zat-zat yang tidak diperlukan tetapi ikut
terlarut dalam cairan penyari, seperti malam dan sebagainya. Proses ekstraksi
berhenti ketika terjadi kesetimbangan antara konsentrasi metabolit dalam pelarut
dan serbuk simplisia (Depkes RI, 1986; Seidel, 2008). Gambar alat maserasi dapat
dilihat pada gambar 2.3.
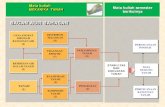
Gambar 2.3. Alat Maserasi (Depkes RI, 1986)
Gambar diatas menunjukkan skema alat maserasi, terdiri dari bejana A yang
terbuat dari gelas, baja tahan karat atau bahan logam lain yang dilapisi email.
Bejana A berpasangan dengan tutup bejana B yang dapat sekaligus dilengkapi
dengan pengaduk C atau dibuat terpisah dengan setiap kali harus membuka tutup
bejana pada waktu akan mengaduk. Dalam hal ini pengaduk C dapat dibuat dari
kayu atau baja tahan karat. Selain itu, dibutuhkan pula bejana lain yaitu bejana D
untuk menampung dan mengendapkan cairan hasil maserasi dari bejana A setelah
disaring atau dituang. Bentuk, ukuran dan bahan bejana D pada dasarnya sama
18
dengan bejana A tetapi tanpa dilengkapi dengan pengaduk. E merupakan alat
penyaring (Depkes RI, 1986).
2.11 Skrining Fitokimia
Skrining fitokimia merupakan tahap pendahuluan dalam penelitian fitokimia.
Skrining fitokimia bertujuan untuk memberikan gambaran mengenai golongan
senyawa yang terkandung dalam tanaman yang diteliti. Metode yang digunakan
dalam skrining fitokimia harus memenuhi kriteria sederhana, cepat, hanya
membutuhkan peralatan yang sederhana, khas untuk satu golongan senyawa, serta
memiliki batas limit deteksi yang cukup lebar (dapat mendeteksi keberadaan
senyawa meski dalam konsentrasi yang cukup kecil) (Kristanti dkk., 2008).
2.12 Kandungan Senyawa Metabolit Sekunder
2.12.1 Tanin
Tanin merupakan senyawa polifenol yang memiliki berat molekul cukup
tinggi. Sifat fisika kimia tanin yaitu membentuk koloid dalam air dan memiliki
rasa asam dan sepat; bersifat polar; larut dalam air, basa encer, alkohol, gliserol
dan aseton; serta jika dicampur dengan alkaloid dan gelatin akan terjadi endapan
(Harborne, 1996).
2.12.2 Saponin
Saponin merupakan golongan senyawa glikosida yang mempunyai struktur
steroid dan triterpenoid. Sifat fisika kimia saponin yaitu mempunyai rasa pahit,
dapat membentuk larutan koloid dalam air dan membuih bila dikocok, bersifat
19
polar, dalam larutan air membentuk busa yang stabil, menghemolisa eritrosit,
merupakan racun kuat untuk ikan dan amfibi, membentuk persenyawaan dengan
kolesterol dan hidrok-sisteroid lainnya, berat molekul relatif tinggi (Harborne,
1996).
2.12.3 Antosianin
Antosianin adalah kelas dari senyawa flavonoid, yang secara luas terbagi
dalam polifenol tumbuhan. Zat tersebut berperan dalam pemberian warna
terhadap bunga atau bagian tanaman lain dari mulai merah, biru sampai ke ungu
termasuk juga kuning. Sifat fisika dan kimia dari antosianin dilihat dari kelarutan
antosianin larut dalam pelarut polar seperti metanol, aseton, atau kloroform,
terlebih sering dengan air dan diasamkan dengan asam klorida atau asam format.
Antosianin stabil pada pH 3,5 dan suhu 35-40°C, mempunyai berat molekul
207,08 gram/mol. Kestabilan antosianin dipengaruhi oleh beberapa faktor antara
lain pH, temperatur, sinar dan oksigen, serta faktor lainnya seperti ion logam
(Harborne, 1996; Widayanti dkk., 2009).
2.12.4 Xanton
Xanton merupakan pigmen kuning fenol yang termasuk kedalam golongan
flavonoid. Xanton mempunyai rumus molekul dasar C13H8O2. Salah satu senyawa
yang termasuk dalam golongan xanton yaitu α-mangostin. Sifat fisiko kimia α-
mangostin ini yaitu berupa serbuk berwarna kuning dengan titik lebur 180-182oC,
stabil pada suhu 65oC, sukar larut dalam air, serta bersifat non polar sehingga
banyak tersari didalam pelarut-pelarut non polar seperti heksan dan kloroform
(Harborne, 1996; Widayanti dkk., 2009; Satong et al., 2011).
20
2.13 Metode Penetapan Kadar Lipid
Dalam penetapan kadar kolesterol total, HDL, LDL dan trigliserida dilakukan
pengukuran dengan metode kalorimetri yang menggunakan alat spektrofotometer.
Spektrofotometer merupakan alat yang digunakan untuk mengukur absorbansi
dengan cara melewatkan cahaya pada panjang gelombang tertentu pada suatu
obyek kaca atau kuarsa yang disebut kuvet. Sebagian dari cahaya tersebut akan
diserap dan sisanya akan dilewatkan. Nilai absorbansi dari cahaya yang
dilewatkan akan sebanding dengan konsentrasi larutan di dalam kuvet.
Keuntungan menggunakan spektrofotometer yaitu untuk analisa membutuhkan zat
dalam jumlah kecil, pengerjaannya cepat, sederhana, cukup sensitif dan selektif
serta mudah dalam interpretasi hasil yang diperoleh (Bassett dkk., 1994; Gandjar
dan Rohman, 2008).
2.13.1 Pengukuran Kadar Kolesterol Total
Penetapan kadar kolesterol total menggunakan metode CHOD-PAP. Kadar
kolesterol ditetapkan setelah terjadi hidrolisis dan oksidasi secara enzimatik.
Indikator yang digunakan yaitu quinonimin yang terbentuk dari hidrogen
peroksida dan 4-aminofenazon dengan adanya fenol dan peroksidase. Reaksi
yang terjadi yaitu :
Ester kolesterol + H2O kolesterol + asam lemak
Kolesterol + O2 kolesten-3-on + H2O2
H2O2 + 4-aminofenazon + fenol quinonimin+ 4H2O
(Dachriyanus dkk., 2007; Prasanth et al., 2012)
kolesterol esterase
kolesterol oksidase
peroksidase
21
2.13.2 Pengukuran Kadar Trigliserida
Penetapan kadar trigliserida menggunakan metode GPO-PAP. Kadar
trigliserida ditetapkan setelah mengalami hidrolisis secara enzimatik dengan
lipase. Indikator yang digunakan yaitu quinonimin yang terbentuk dari hidrogen
peroksida, 4-aminoantipirin, dan 4-klorofenol dengan adanya pengaruh katalis
peroksidase. Reaksi yang terjadi yaitu :
Trigliserida gliserol + asam lemak
Gliserol + ATP gliserol-3-fosfat + ADP
Gliserol-3-fosfat + O2 dihidroksiaseton fosfat + H2O2
2H2O2 + 4-aminoantipirin + 4-klorofenol quinonimin+HCl + H2O
(Dachriyanus dkk., 2007; Prasanth et al., 2012)
2.13.3 Pengukuran Kadar HDL
Pengukuran kadar HDL dilakukan dengan metode enzimatik CHOD-POD.
Serum yang diperoleh diendapkan dengan asam fosfotungestik dan magnesium.
Setelah disentrifugasi, HDL dalam supernatan ditambahkan dengan reagen
diagnostik kit (Dachriyanus dkk., 2007; Prasanth et al., 2012).
2.13.4 Perhitungan Kadar LDL
Kadar LDL dihitung dengan menggunakan rumus Friedewald setelah kadar
kolesterol total, trigliserida dan HDL diukur. Rumus yang digunakan yaitu :
LDL (mg/dl)= kolesterol total - trigliserida - HDL
5
(Widiastuti, 2003; Dachriyanus dkk., 2007)
Gliserol kinase
Gliserol-3-fosfat oksidase
Lipase
peroksidasee




























![BAB II - Tinjauan Pustaka [Revisi 040712]](https://static.fdokumen.site/doc/165x107/55cf9766550346d033916bfb/bab-ii-tinjauan-pustaka-revisi-040712.jpg)






