Protein
-
Upload
mita-megah -
Category
Science
-
view
60 -
download
0
Transcript of Protein


PROTEIN
Biopolimer yang terdiri dari banyak satuan Asam Amino yg dihubungkan oleh ikatan peptida.
Fungsi:
a. Beberapa protein merupakan komponen utama dalamjaringan struktur (otot, rambut, kuku, kulit)
b. Sebagai protein aktif [enzim, hormon, haemoglobin, toksin dll ]

Sifat-sifat protein
1. IonisasiProtein yang larut dalam air dalam suasana asam akanmembentuk ion (+) sedangkan dalam suasana basaakan membentuk ion (-).
2. DenaturasiPerubahan konformasi alamiah menjadi suatukonformasi yang tidak menentu.*perubahan suhu, pH atau reaksi dengansenyawa lain

Penggolongan Protein
• Protein Fibrous (Serat)
Protein yang terdapat pada hewan, tidak larut dalam
air. Misal : keratin, kolagen, sutra
• Protein Globular
Protein yang larut dalam air. Misal : enzim, hormon,
hemoglobin, mioglobin, ovalbumin (pada putih telur)

Struktur Protein
1. Struktur primer protein
merupakan struktur yang sederhana dengan urutan-urutanasam amino yang tersusun secara linear yang mirip sepertitatanan huruf dalam sebuah kata dan tidak terjadipercabangan rantai.
2. Struktur sekunder protein merupakan kombinasi antara struktur primer yang linear distabilkan oleh ikatan hidrogen antara gugus =CO dan =NH di sepanjang tulang belakang polipeptida.

3. Struktur tersier protein adalah lapisan yang tumpang tindih di atas pola struktursekunder yang terdiri atas pemutarbalikan takberaturan dari ikatan antara rantai samping (gugus R) berbagai asam amino.
4. Struktur kuarterner protein adalah gambaran dari pengaturan sub-unit ataupromoter protein dalam ruang. Struktur ini memilikidua atau lebih dari sub-unit protein dengan strukturtersier yang akan membentuk protein kompleks yang fungsional.

Bentuk struktur primer Bentuk struktur sekunder
Bentuk struktur tersier Bentuk struktur kuartener

Asam amino adalah senyawa penyusun protein. Asam amino mempunyai satu gugus karboksildan satu gugus amino. Pada umumnya gugusamino terikat pada posisi dari gugus karboksil.
R CH COOH
asamNH2
basa
R CH COO-
NH3
asam -amino ion switter pH : 7,4
(Amfoter)
R H, C - : kiral
ASAM AMINO???
Gugus karboksil
Gugus amino

Struktur Asam Amino
Suatu asam amino-α terdiri atas:
Atom C α. Disebut α karena bersebelahan dengan gugus karboksil (asam).
Atom H yang terikat pada atom C α.
Gugus karboksil yang terikat pada atom C α.
Gugus amino yang terikat pada atom C α.
Gugus R yang juga terikat pada atom C α.

C
COO-
CH2OH
+H3N H C
COO-
CH2OH
NH3+H
L-serine D-serine
CONTOH ASAM AMINO
Didasarkan pada struktur D – gliseraldehidjika gugus NH3
+ terletak disebelah kanan diberi awalan DSedangkan jika NH3
+ dikiri diberi awalan L

Sifat-Sifat Asam Amino
1. Umumnya larut dalam air, namun tidak larut dalampelarut organik non-polar seperti eter aseton dankloroform
2. Asam amino memiliki titik lebur yang lebih tinggidibandingkan dengan asam karboksilat dan amina
3. Asam amino bersifat amfoter yang dapat berperansebagai asam (mendonorkan proton pada basa kuat) dan dapat berperan sebagai basa (menerima proton dari asam kuat)

Penggolongan Asam Amino
Penggolongan asam amino didasarkan pada sifat dari rantaisamping (-R). Berdasarkan sifat rantai samping R, asamamino dapat digolongkan menjadi :
1. Asam amino dengan R non polar [hidrofobik]
2. Asam amino dengan R polar tidak bermuatan
3. Asam amino dengan R polar bermuatan (+) atau (-)

• Muatan total asam amino dalam larutan akan menentukankelarutannya, sebagai fungsi pH. pH dimana asam amino mempunyai muatan = 0 (tidak bermuatan) disebut pH isoelektrik (pI). Pada pI, kelarutan asam amino <<<, olehkarena itu pada pI asam amino akan mengendap.
• pH isoelektrik untuk asam amino dengan R tidakterionisasi berkisar 5.5 – 6.5. pH isoelektrik untuk asamamino dengan R terionisasi.

pH Isoelektrik Asam Amino
Asam Amino Gugus Terionisasi pH Isoelektrik
As. Aspartat Karboksil 2,98
As. Glutamat Karboksil 3,08
Histidin Imidazol 7,64
Sistein Tiol 5,05
Tirosin Fenol 5,63
Lisin Amino 9,47
Arginin Amino 10,76

Fungsi pH Isoelektrik (pI)
– Untuk mengkristalkan asam amino/protein pengendapan isoeletrik
– Dengan mengetahui titik isoelektrik dapat meramalkan proses migrasi protein dalam medan elektrikum Dasar untuk pemisahan asam amino dengan elektroforesis

Macam Asam AminoAda 20 macam asam amino, yang masing-masing ditentukan oleh jenis
gugus R atau rantai samping dari asam amino. Jika gugus R berbedamaka jenis asam amino berbeda.
No Nama Singkatan
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
Alanin (alanine)
Arginin (arginine)
Asparagin (asparagine)
Asam aspartat (aspartic acid)
Sistein (cystine)
Glutamin (Glutamine)
Asam glutamat (glutamic acid)
Glisin (Glycine)
Histidin (histidine)
Isoleusin (isoleucine)
Leusin (leucine)
Lisin (Lysine)
Metionin (methionine)
Fenilalanin (phenilalanine)
Prolin (proline)
Serin (Serine)
Treonin (Threonine)
Triptofan (Tryptophan)
Tirosin (tyrosine)
Valin (valine)
Ala
Arg
Asn
Asp
Cys
Gln
Glu
Gly
His
Ile
Leu
Lys
Met
Phe
Pro
Ser
Thr
Trp
Tyr
Val

Ikatan Peptida
• Ikatan yang menghubungkan 2 asam amino melaluigugus karboksil dari satu asam amino dengan gugusamino dari asam amino yang lain.
+H3N CH2 C O-
O
+H3N CH CO
OCH3
glysin alanin
+
+H3N CH2
CHN
O
C C O-
O
+ H2O
CH3
ikatan peptida
gly - ala(glysinalanin)
C-terminalN-terminal

Berdasarkan konvensi ikatan peptida ditulis denganasam amino yg mempunyai NH3
+ bebas (sebelah kiri) dan Asam Amino dengan gugus COO- bebas (sebelahkanan).
Molekul yang mengandung 2 asam amino dengan 1 ikatan peptida disebut dipeptida.
Molekul mengandung 3 asam amino disebut tripeptida. Selanjutnya terdapat pula tetrapeptida, pentapeptida, dst.
Lanjutan…

Pemisahan Protein dan Asam Amino
a. ElektroforesisCara ini didasarkan pada kecepatan bergerak yang berbeda-beda dari protein dalam medan listrik, padapH tertentu.
b. KromatografiPenentuan dan pemisahan campuran protein dengancara kromatografi dilakukan berdasarkan prinsip-prinsip kromatografi pada umumnya yaitu denganmempertimbangkan adanya dua fase yaitu fase gerakdan fase diam.
c. Pengendapan protein sebagai garamSebagian besar protein dapat diendapkan dari larutanair dengan penambahan asam tertentu, seperti, asamtrikloroasetat dan asam perkolat.

• Enzim merupakan biokatalisator yang mempercepatjalannya reaksi tapa ikut bereaksi. Enzim yang berfungsisebagai biokatalisator tersusun atas senyawa protein dannon protein karena umumnya tidak dapat bekerja tanpaadanya suatu zat non protein tambahan yang disebutkofaktor.
Sifat :Thermolabil. Mudah rusak bila dipanskan lebih dari 60CMerupakan senyawa protein, sehingga sifat protein masihmelekat pada enzim
Sebagai biokatalisator , reaksinya menjadi sangat cepatdan berulang ulang. Bekerja didalam sel (endoenzim) dandiluar sel (ektoenzim)
Apa sih enzim dan koenzim itu???

Secara kimiawi enzim tersusun atas dua bagian, yaitu bagian
protein (apoenzim) dan bagian bukan protein (gugus
prostetik).
Apoenzim merupakan bagian enzim aktif yang tersusun atas
protein dan mudah berubah (labil) terhadap faktor
lingkungan, misalnya pH dan suhu.
Sedangkan gugus protestik merupakan gugus yang tidak aktif,
berupa unsur–unsur logam, seperti besi, mangan,
magnesium, atau natrium yang disebut kofaktor. Gugus
prostetik juga dapat berupa bahan organik bukan protein,
seperti vitamin B yang disebut Koenzim.

ENZIM
Penggolongan dan tata nama enzim
1. Tata nama berdasarkan substrat
Jika dikatalis adalah glukosa: enzim glukase
2. Tata nama berdasarkan jenis ikatan kimia substrat
Jika dikatalis ikatan peptida: enzim peptidase
Jika dikatalis ikatan ester: enzim esterease
Jika dikatalis ikatan nukleotida: enzim nukleotidase
3. Tata nama berdasarkan jenis reaksi
Untuk mengoksidasi glukosa: enzim glukosa oksidaseEnzim yang mengkatalis pemindah gugus dinamai : tranferase, contoh untuk memindahkan gugus NH2: enzim lebih khas dinamai: enzim amino transferase
Nama tiap enzim disesuaikan dengan nama substratnyadengan penambahan ase di belakangnya

Kelas Tipe reaksi
OksidoreduktaseEnzim yang mengkatalis reaksi oksidasi-reduksi(memsahkan dan menambahkan elektron atauhidrogen)
Transferase(Kinase)
Memindahkan gugus senyawa kimia
Hidrolase(protease, lipase, amilase)
Enzim yang mengkatalis reaksi hidrolisis (memutuskan ikatan kimia dengan penambahan air)
Ligase(fumarase)
Mengkatalis reaksi pengabungan dua senyawa yang disertai perurairan molekul ATP (membentuk ikatan rangkap)
Isomerase(epimerase)
Mengkatalisir perubahan isomer
Polimerase(tiokinase)
Menggabungkan monomer-monomer sehinggaterbentuk polimer

Faktor Yang Mempengaruhi KerjaEnzim
Selain adanya zat penghambat (inhibitor), kerja enzim dapatdipengaruhi oleh beberapa faktor antara lain:
1. Zat-zat pengaktif (aktivator)Zat-zat kimia tertentu dapat memacu atau mengaktifkan kegiatanenzim. Contoh: garam-garam dari logam alkali dan logam alkali tanahdengan konsentrasi encer, ion kobalt (Co), mangan (Mn), nikel (Ni), magnesium (Mg), dan klor (Cl).
2. SuhuSetiap enzim mampu bekerja secara efektif pada suhu tertentu danaktivitasnya akan berkurang apabila berada pada kondisi di bawahatau di atas titik tertentu, suhu optimal yang mendekati suhu tubuh(35o C - 40oC). Enzim dapat rusak pada suhu tinggi (>50oC), dan padasuhu rendah (0oC), enzim menjadi tidak aktif.

3. pHSebagaimana faktor suhu, enzim juga mempunyai pH tertentu agar dapat bekerja secara efektif. Enzim dapat bekerja optimal pada pH netral (pH = 7), pH basa (>7) atau pH asam (<7) tergantung pada jenisenzim masing-masing
4. Konsentrasi enzim
Konsentrasi enzim yang tinggi akan mempengaruhi kecepatan reaksisecara linear (kecepatan bertambah secara konstan)
5. Konsentrasi substratPada konsentrasi substrat yang rendah, kenaikan substratakan meningkatkan kecepatan reaksi enzimatis hampir secara linear. Jika konsentrasi substrat tinggi, maka peningkatan kecepatan reaksienzimatis akan semakin menurun sejalan dengan peningkatan jumlah
substratnya.

Penghambatan aktifitas enzim
ada dua tipe:
1. Kompetitifzat penghambat mempunyai struktur yang miripdengan substrat sehingga dapat bergabung dengansisi aktif enzim. Terjadi kompetisi antara substratdengan inhibitor untuk bergabung dengan sisi aktifenzim (misal feed back effect)
2. Non kompetitifzat penghambat menyebabkan struktur enzimrusak sehingga sisi aktifnya tidak cocok lagi dengansubstrat

DENATURASI
Jika struktur enzim berubah sehingga substrattidak dapat terikat, maka aktivitas katalisis enzimhilang dan dikatakan terjadi denaturasi enzim.
Pada umumnya denaturasi menyebabkan enzimtidak dapat kembali
Beberapa faktor yang menyebabkan denaturasienzim:
1. suhu tinggi2. Oksigen atau bahan pengoksidasi lainnya3. Bahan pereduksi4. Kation logam berat (Ag+, Hg2+, Pb2+)

FUNGSI DAN MEKANISME KERJA ENZIM
Enzim sebagai protein katalis
Dixon dan Webb, mendefinisikan enzim sebagai suatuprotein bersifat katalis. Definisi ini disebabkan olehkemampuannya untuk mengaktifkan senyawa lain secaraspesifik.
Definisi lain: enzim adalah suatu katalisator protein yang mempercepat reaksi kimia dalam sistem biologis.

Lanjutan…
Interaksi yang spesifik dari enzim dengan suatumolekul tertentu dan menyebabkan pengaktifan molekultersebut selanjutnya mengakibatkan perubahan struktursehingga menimbulkan gagasan akan substrat.
Substrat didefinisikan sebagai senyawa yang dikenalisecara spesifik oleh enzim dan selanjutnya diaktifkansehingga mengalami perubahan kimia.
Mengingat demikian spesifik interaksi antara substrat dan enzim, maka bagian tersebut dinamai sebagai situs aktif(active site) atau lebih tepat lagi situs katalitik(catalytic site)

Pada umumnya terdapat 2 mekanisme kerja enzim mempengaruhi reaksi katalisis
1. enzim meningkatkan kemungkinan molekul-molekul yang bereaksi saling bertemu dengan permukaan yang salingberorientasi.
Hal ini terjadi karena enzim mempunyai afinitas yang tinggi terhadap substrat dan kemampuan mengikatnyawalaupun sementara
2. Pembentukan ikatan yang sementara (non kovalen) antarasubstrat dengan enzim menimbulkan penyebaran elektrondalam molekul substrat dan penyebaran ini menyebabkansuatu regangan pada ikatan kovalen spesifik dalam molekul substrat sehingga ikatan kovalen tersebut menjadi mudahpecah

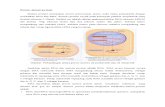
Grafik Michaelis-Menten

Grafik Lineweawer-Burk

Isoenzim???
Teknik pemisahan protein dilakukan dengan metode elektroforesis yaitupemisahan protein terlarut atau molekul bermuatan lainnya dalam medanlistrik.
Dengan teknik ini diketahui bahwa lebih dari satu enzim yang dapat bereaksidengan substrat yang sama dan mengubahnya menjadi produk yang sama.Enzim ini dinamakan isoenzim
Pentingnya isoenzim : perbedaan respons isozim terhadap faktor lingkunganjika lingkungan berubah isozim yang paling aktif tersebut melaksanakanfungsinya dan membantu organisme untuk bertahan hidup

Aplikasi enzim di bidang medis
Kalangan kedokteran dan kedokteran hewan memanfaatkan
pengetahuan enzim untuk tujuan DIAGNOSIS dan PENGOBATAN
Wolgemuth (1908):
-> Enzim amilase dalam urine, meningkat jumlahnya pada radang
pankreas
Kay, Kings, Bodansky dan Roberts (1920-1930):
-> Enzim fosfatase alkali, penyakit hati