sintesis bhn tak organik
-
Upload
adhirohadhi -
Category
Documents
-
view
416 -
download
7
Transcript of sintesis bhn tak organik

http://institut.fs.utm.my/~ramli/
SINTESIS BAHAN TAK ORGANIK
SINTESIS BAHAN TAK SINTESIS BAHAN TAK ORGANIKORGANIK

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 1
Sintesis Bahan Tak Organik
Berbeza dengan kaedah lazim digunakan dalam kimia organik,kimia organologam dan kimia koordinatan kerana dalam sintesi bahan tak organik (pepejal) kebanyakannya merupakan usaha memanjangkan kekisi, iaitu membina kekisi atau mengubahsuai kekisi.
Kaedah suhu tinggi (kaedah seramik)
Kaedah ini paling banyak digunakan untuk menyediakan bahan tak organik pepejal.
Dasarnya: Tindak balas komponen pepejal dalam nisbah molaryang betul pada suhu tinggi dalam tempoh yang lama (panjang).
Kaedah ini banyakdigunakan untuk mesintesis oksida logam, kalkogenida(sulfida, selenida, tellurida) dan pniktida (fosfida dan nitrida), silikat danfosfat.
Sukatan/timbangan bahan pemula yg tepat tersangat penting kerana bahan tidak dapat ditulenkan selepas disintesis.

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 2
Atas alasan yg serupa, pemilihan reaktan adalah penting.
Awas!1. Jangan gunakan bahan pemukla yg higroskopik (menyerap air) atau yg tak-
berstoikiometri (komposisi berubah-ubah).
2. Elak menggunakan reaktan yg mudah mengwap atau sensitif udara (Jikatak ada pilihan gunakan kaedah tiub kedap (sealed tube).
• Tindak balas keadaan pepejal memerlukan suhu tinggi; kadang-kadang mencecah 2000 oC.
• Dengan itu, radas kaca biasa tidak sesuai digunakan (kaca borosilikat lembek di atas 600 oC).
• Jadi, gunakan bahan yg tinggi takat lebur, seperti kapsul atau mangkuk pijar diperbuat drp logam mahal (Pt, emas), alumina atau zirkonia.

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 3
berbagai mangkuk pijar
Kaca borosilikat (pyrex) 575 820Tiub emas 1013 1063Silika (kuatza) 1405 1853Platinum 1719 1769Alumina (Al2O3) 1900 2072Zirkonia (ZrO2) 2000 2700Magnesia (MgO) 2400 2852
Mangkuk/bekas suhu maks*. oC takat lebur, oC

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 4
Pemanasan suhu tinggi
Gunakan relau (furnace)
Relau komersial bolehmencapai suhu 2000 oC.
Suhu yg lebih tinggi,katakan 4000 oC, bolehdiperoleh menggunakanlaser.
relau kotak (box/muffle furnace)
relau tiub (tube furnace)

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 5
Contoh sintesis
Suhu tindak balas kimia oksida ialah dalam julat 500 – 2000 oC
Na2O2 + 2CuO 2NaCuO2 (suhu 400 oC)
MgO + Al2O3 MgAl2O4 (suhu 1400 oC)
3CsCl + 2ScCl3 Cs3Sc2Cl9
NaAlO2 + SiO2 NaAlSiO4

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 6
Proses tindak balas di antara pepejal-pepejal
Skema zarah-zarah bertindak balasdalam tindak balas keadaan pepejal
Campuran tindak balas terdiri drp longgokan atau himpunan zarah-zarah pepejal terpisah oleh ruang-ruang kosong tetapi terdapat zarah-zarah bersentuhan di satah-satah hablur tertentu.
Menambahkan titik sentuhan antaramuka zarah-zarah dalam campuran bolehmencepatkan tindak balas.
Ini boleh dicapai dengan:• Mengisar semula campuran secara berkala untuk meningkatkan kehomogenan,
katakan selepas setiap 16 – 24 jam.
• Meningkatkan sentuhan antara zarah dengan memaksa zarah mendekati satusama lain, misalnya menekan campuran menjadi pelet untuk mengurangkan ruang kosong.
• Meningkatkan suhu untuk memberi tenaga kepada zarah untuk bergerak.

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 7
Skema tindak balas pembentukan LaFeO3
• Secara amalan, ketiga-tiga cara di atas diguna pakai.
• Proses mengisar semula dan pemanasan sering dirujuk sebagai kaedah “goncang dan bakar”.
• Mendapatkan keadaan annealing dan suhu lazimnya secara “trial and error” kerana penyediaan bahan baru sukar diramalkan.Seringkali komposisi produk tidak sentiasa homogen, walaupun tindak balas berjalan hampir selesai sepenuhnya. Jika terdapat bendasing tertinggal apabila tindak balasselesai, lazimnya bendasing itu sukar disingkirkan.
Untuk mengatasi pembauran yg perlahan, saiz zarah harus dikecilkan (mengisar secara mekanikal mencapai saiz zarah di antara 10,000 dan 100,000 A, iaitu sekitar 1000 – 10,000 sel unit.
Kaedah berikut dapat mencipta pemula (precursor)dgn cara pemelarutan dalam pelarut yg sesuai. Caraini mengizinkan pencampuran pada skala atom,sebelum pelarut disingkirkan, meninggalkanpepejal-pepejal yg telah bercampur sempurna, dansaiz zarah yg lebih kecil.
Residu yg diperoleh kemudian dipanaskan dengan kaedah seramik, tetapi suhu tindak balas lazimnya akan jauh lebih rendah.
Skema tindak balas bagi pembentukan lantanum besi oksida dengan kaedah seramik

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 8
Pengeringan sembur dan sejukbeku (Spray and freeze drying)
Dalam kedua-dua kes, reaktan dilarutkan ke dalam pelarut biasa.
Kemudian sama ada disembur ke dalam kebuk panas, di mana pelarut akan terwap serta merta (pengeringan sembur), atau
Disejukbekukan di dalam cecair nitrogen dan pelarut disingkirkan pada tekanan rendah (pengeringan sejukbeku).
Pemelarutan garam logam
Kaedah ini melibatkan pemelarutan garam logam (lazimnya nitrat, hidroksida atau oksalat) di dalam pelarut yg sesuai, dan campuran diwapkan sehingga kering.
Residu kering kemudian ditindakbalaskan seperti dalam kaedah seramik.
Prosedur ini baik jika komponen-komponen mempunyai kelarutan yangserupa; jika tidak pepejal yg kelarutan lebih rendah akan mula termendak dahulu. Akibatnya pencampuran yg terhasil tidak akan lebih baik daripada kaedah seramik.

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 9
Ko-pemendakan
Larutan campuran ion boleh dimendakkan bagi menghasilkan suatupepejal yang mengandungi ion-ion yg dikehendakki.Walau bagaimanapun, mestilah berhati-hati supaya ion-iontermendak mengikut nisbah yg dikehendakki.
Misalnya, asid oksalik boleh digunakan untuk memendakkkan ionzink oksalat daripada larutan ion-ion berkenaan yg terlarut dalam asid asetik.
Zn2+ (ak) + 2Fe2+ (ak) + 3C2O42+ (ak) ZnFe2(C2O4).6H2O
ZnFe2O4 spinel akan terhasil apabila mendakan tersebut dipanaskan sehingga 800 oC.
Walaupun kaedah ini mengizinkan penurunan suhu pembakaranyang banyak berbanding kaedah seramik, ianya amat sukardigunakan bagi sistem banyak ion.

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 10
Kaedah sol-gel
Kaedah ini juga penting dan digunakan secara meluas dalam penyediaan zeolit, filem tipis dan .
Prosesnya melibatkan penyediaan larutan pekat (sol) komponen-komponen tindak balas.
Campuran ini kemudian diubah menjadi gel yg hampir tegar dengan cara menyingkirkan pelarut atau dengan menambahkan komponenyang membuatkan gel menjadi pepejal.
Gel itu kemudian dirawat dgn cara tertentu untuk menghasilkan bahan yg diingini.
Kaedah ini boleh juga digunakan untuk menyediakan bahan komposit, di mana spesies organik dan tak organik bolehdiperangkap di dalam matrik lengai.
Sifat kedua-dua matriks lengai dan spesies terperangkap tergabung dalam produk yg terhasil.
salutan abrasif

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 11
Contoh sintesis
3KF(ak) + MnCl2(ak) KMnF3(p) + 2KCl(ak)
ZrO2 + 2H3PO4 Zr(HPO4)2.H2O + H+O
12NaAlO2 + 12Na2SiO3.9H2O Na12[Si12Al12O48].nH2O + 24NaOH
zeolit 4A

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 12
Kaedah Tiub Kedap (Sealed tubes)
Pada kes tertentu, tindak balas secara terus dalam keadaan ambien(dalam udara pada tekanan atmosfera) untuk membentuk sesuatu bahan tidak boleh dilakukan.
Ini mungkin kerana beberapa sebab, termasuk reaktan mudahmengwap, bahan pemula dan/atau produk sensitif terhadap udara, atau keinginan membuat sebatian dengan logam bernombor pengoksidaan luar biasa rendah.
Contoh sintesis
Serbuk mangan dan sulfur akan bertindak balas pada 500 oC untukmembentuk MnS
Mn (p) + S (p) MnS (p)
Tetapi, jika dipanaskan dalam udara pada suhu ini kesemua sulfurakan terwap pada 110 oC.
Supaya mangan dan sulfur sentiasa berada berhampiran, kedua-duanya mesti ditindak balaskan di dalam bekas kedap.

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 13
Penyediaan sebatian talium(I) TlTaO3 gas lengai digunakan untukmengekang pengoksidaan.
Tl2O + Ta2O5 2TlTaO3
Begitu juga penurunan V2O5 menjadi VO2
V2O5 VO2
Sintesis kalsium emas nitrida dilakukan dalam tiub kedap emas berisi gas nitrogen
2Ca3N2 + 2Au 3Ca2AuN + ½N2
N2, 600 oC
H2, 1000 oC
N2

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 14
Kaedah Atmosfera Terkawal
Ada bahan yang tak dapat dijana secara pemanasan dalam udara pada tekanan satu atmosfera.
Bahan-bahan seperti ini disediakan dalam keadaan atmosfera terkawal.
Contoh sintesis
Oksida vanadium yang sedia ada ialah V2O5. Untuk menyediakan VOdimana vanadium berada dalam no. pengoksidaan +2, memerlukan hidrogen dilalukan pada V2O5 pada 1000 oC.
Sintesis dalam vakum kerana ada reaktan yang mengwap pada suhu tindak balas
Ta + S2 TaS2
Tl2O3 + 2BaO + 3CaO + 4CuO Tl2Ba2Ca3Cu4O12
vakum, 500 oC
vakum, 860 oC

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 15
Menyediakan sebatian yang mengandungi nikel dalam keadaanpengokdsidaan +3, seperti LaNiO3, memerlukan annealing(rawatan haba) dgn oksigen, kerana dalam keadaan biasa nikel akan berada pada no. pengoksidaan +2.
LaNiO 2.5 (p) LaNiO3 (p)
Disini, LaNiO 2.5 adalah tak stoikiometri. Bermaksud, tak semua tapak yg ada didalam kekisi dipenuhi; akibatnya menghasilkan bilangan atom yang tak bulat (non-integral) dalam formulakimianya
Perhatian: Ketak stoikiometrian dalam sebatian keadaan pepejal boleh memberi kesan kepada keadaan penyediaan dansifat fizik bahan berkenaan.

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 16
Sampel yg disediakan pada suhu tinggi dan dilindap (disejukkan dgn deras)lazimnya “tak teratur” (diordered), lebih-lebih lagi jika fasanya takstoikiometri. Maka, proses annealing (proses menyejukkan secara perlahan-lahan) dilakukan atau dipilih kerana tindak balas annealing berlaku pada suhu lebih rendah drp suhu penyediaan awal,.
Annealing digunakan untuk berbagai bahan untuk menyingkirkan kecacatan,meningkatkan kehomogenan dan mengurangkan tegasan.
Sementara penyediaan fasa dilakukan dalam relau kotak, tindak balas annealing dilakukan dalam relau tiub dilengkapi dengan tiub seramik atau silika untuk mengizinkan gas dilalukan kepada campuran.
Tindak balas annealing relau tiub

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 17
Kaedah Hidroterma
Tindak balas terus untuk menyediakan bahan tak larut boleh dilakukan melalui tindak balas hidroterma.
Tindak balas jenis ini amat bergunakan untuk menyediakan bahan-bahan aluminosilikat yang juga dikenali sebagai zeolit.
Zeolit dibentuk daripada sumber-sumber aluminium dan silikon yangdipanaskan dengan kehadiran agen templat (anion atau kation dengan bentuk tertentu).
Kaedah Tekanan Tinggi
Kimia tekanan tinggi merupakan suatu kegiatan yang mahal dan merbahaya.Namun begitu, ganjaranya juga tinggi.
Keadaan seperti ini akan mengizinkan keadaan pengoksidaan dan strukturyang luar biasa tercapai. Keadaan tekanan tinggi memihak kepada strukturyang tumpat.
Kaedah ini mengizinkan sintesis sebatian-sebatian yang tidak dapat dibuat dengan cara lain.

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 18
Hablur tunggal
Kebanyakan teknik menghasilkan hablur tunggal dalam sistem molekul tak boleh digunakan kepada bahan keadaan pepejal. Misalnya, oksida keadaan pepejal seperti bahan-bahan spinel (AB2O4) tak larut dalam sebarang pelarut pada sebarang suhu, jadi tak boleh ditumbuhkan memelalui pemejalan.
Walau bagaiamanapun, terdapat dua kaedah yang sering digunakan untukmenghasilkan hablur tunggal daripada bahan pepejal.
Pemejalan daripada leburan
Terdapat beberapa cara menghasilkan hablur tunggal daripada leburan.Bahan pepejal dipanaskan dalam mangkuk pijar sedikit melebihi suhu leburnya. Kemudian hablur ditumbuhkan sama ada melalui penyejukan perlahan atau penonjolan permukaan.
Kaedah tarik
Bahan diletakkan ke dalam mangkuk pijar lengai dan dipanaskan sedikit di atas suhu leburnya. Hablur benih diletakkan di permukaan leburan danperlahan-lahan ditarik keluar daripada leburan. Hablur akan tumbuh berterusan di antaramuka.

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 19
Zon terapung
Sebatang rod bahan dipegang tegak dan dipanaskan di satu hujungnya sehingga berlaku leburan. Dengan menjauhkan sumber haba di sepanjangrod, peleburan dan penghabluran semula berlaku semasa sumber haba dianjakkan. Dengan meletakkan hablur benih di sebelah hujung rod,keseluruhan rod akan diubah menjadi hablur tunggal.
Cerunan suhu
Kecerunan besar suhu dicipta di sepanjang sampel supaya hablur membenihdan tumbuh bermula di bahagian mangkuk pijar yang lebih sejuk.
Lakuran nyala
Pepejal diletakkan ke dalam “hopper”, dipanaskan dengan api oksi-hidrogen dan dibiarkan menitis jatuh ke atas hablur benih. Kaedah ini lazimdigunakan untuk membuat batu permata sintetik seperti batu permatanilam (sapphire) kerana bahan mempunyai takat lebur yang sangat tinggi.
Tetapi kaedah ini hanya sesuai untuk pepejal yang melebur untukmembentuk satu fasa.
Untuk sistem fasa berbilang, gambarajah fasa hendaklah dikaji dahuluuntuk memastikan stoikiometri yang betul terhasil pada suhu yang dijana.

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 20
Kaedah larutan
Kaedah ini serupa dengan kaedah yang digunakan dalam sintesis hidroterma biasa, kecuali larutan di sini adalah lampau tepu dan bekas disejukkan dengan amat perlahan-lahan (1 oC per minit) untukmemudahkan hablur besar tumbuh.
Bahan nano
Bahan nano adalah gugusan kecil bahan yang mempunyai sifat tertentu berbeza daripada spesies molekul dan bahan bertertib julat panjang.
Lazimnya, gugusan ini terbentuk kerana perubahan keadaan yangmengejut, misalnya cecair pepejal, terdiri daripada 500 unit dan saiz50 –200 Å.
Sifat fizik bahan seperti ini menunjukkan sisihan daripada bahan pukal.Misalnya, sifat magnet bahan nano besi oksida lebih lemah daripada bahan pukalnya. Perkara ini juga benar bagi logam semikonduktor calkogenida(sebatian logam berat unsur Kumpulan 16).

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 21
Bahan Amorfus
Kebanyakan bahan dapat disediakan dalam keadaan amorfus.
Prinsip yang terlibat ialah pelindapan pantas. Cara ini dapat menghalang bahan daripada menghablur dengan cara yang tertib. Ini boleh dicapai melaui proses penyejukan lampau, pemendakan wap, dan pengelan.Kaedah ini menghasilkan pepejal yang tidak mudah diciri dengan teknikbiasa seperti penyerakan sinar-x.
Pemendakan wap merupakan cara yang paling lazim digunakan untukmenghasilkan bahan amorfus. Dengan kaedah ini bahan diwapkan dankemudian dimendakkan di atas suatu permukaan pada suhu yang sangat rendah. Cara ini sama seperti kaedah pengeringan beku. Apabila berada di atas permukaan, bahan tersebut dibiarkan menghablur dengan cara memanaskan permukaan berkenaan.
Kaca berketumpatan rendah, dengan stoikiometri yang tepat, bolehdisediakan dengan kaedah sol-gel. Menggunakan reagen organik, suatuaerogel boleh dibentuk daripada sol. Menyingkirkan reagen organiknya menghasilkan kaca terkembang.

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 22
Gambarajah fasa dan Tindak balas Leburan
Tindak balas keadaan pepejaltersangat perlahan. Boleh tak kalau dileburkan bahan-bahan bersama-sama dan cepatkan segala-galanya?
Malangnya, jarang sekali dua bahan A dan B yang lebur bersama-sama lalu membentuk pepejal AB apabila sejuk. Proses begini dinamakan peleburan serbasama (congruent melting) danbermaksud ABcecair menjadi ABpepejalapabila sejuk.
Kebanyakan bahan melebur takserbasama (incongruently) di mana satu komponen menghablur dahulu apabila sejuk lalu meninggalkan cecair yg lebih kaya dengan komponen yangsatu lagi.
Penyejukan bahan-bahan jenis ini menghasilkan campuran A, AB dan B.
Cecair AB
Cecair ABCecair BPepejal A
Cecair BPepejal ABPepejal A
Pepejal AB Pepejal BPepejal ABPepejal A
serbasama tak serbasama

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 23
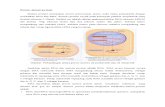
Gambarajah fasa digunakan untuk menyiasat pemisahan spesies pada suhu tertentu.
Gambarajah fasa bagi dua pepejal A dan B yang saling tidak bertindak balasditunjukkan di atas. Titik X ialah titik eutektik, iaitu suhu terendah di mana kesemua sistem berada dalam keadaan leburan.
Garis lengkung yang memisahkan daerah pepejal dengan cecair dipanggil liquidus.
Oleh kerana A dan B tidak bertindak balas, tidak ada garis tegak di dalam gambarajah.

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 24
Gambarajah fasa di atas adalah bagi sistem pepejal A dan B yangbertindak balas lalu membentuk AB dan sebatian AB melebur serbasama.
Menaikkan suhu melebihi T1 dengan nisbah A dan B sama (50:50)menghasilkan pepejal AB apabila disejukkan.
Pastinya, bergerak ke kanan akan menghasilkan campuran AB dan B.

kimia bahan©2002 ramlihitam SINTESIS BAHAN TAK ORGANIK PEPEJAL 25
Gambarajah fasa di atas adalah bagi sistem pepejal A dan B yang bertindakbalas lalu membentuk AB, dan sebatian AB melebur tak serbasama.
Menyejukkan campuran AB 50:50 daripada keadaan cecair, mula-mula pepejal Aakan termendak (bawah suhu T3), kemudian bawah suhu T2 AB mula termendak.Walau bagaimanapun, cecair itu kini kaya dengan B.
Jadi, dengan kadar penyejukan yang berpatutan, campuran produk pepejal, A, AB dan B, akan diperoleh.Dalam kes ini, elok suhu dibiarkan bawah T2 yang juga dipanggil suhu peritektik.
Ini bermakna campuran melebur tak serbasama tidak boleh dibenarkan leburdan sintesis mesti dilakukan dalam keadaan pepejal.