BAB II KAJIAN PUSTAKA 2.1.1 Lapisan Air Mata II.pdf · 0,2 µm dan merupakan lapisan yang terletak...
Transcript of BAB II KAJIAN PUSTAKA 2.1.1 Lapisan Air Mata II.pdf · 0,2 µm dan merupakan lapisan yang terletak...

8
BAB II
KAJIAN PUSTAKA
2.1 Anatomi dan Fisiologi Lapisan Air Mata dan Kelenjar Meibom
2.1.1 Lapisan Air Mata
Permukaan bola mata dilindungi oleh lapisan air mata yang berfungsi
mempertahankan kelembaban permukaan mata, sebagai media pembersih dari
debris, melindungi permukaan mata, dan menyediakan oksigen dan nutrisi kepada
epitel kornea. Lapisan air mata mengangkut zat-zat dan debris kemudian dikeluar
melalui pungtum lakrimal. Sebagai tambahan lapisan air mata juga mengandung
bahan-bahan antimikroba, sebagai lubrikasi antara kornea dan kelopak mata serta
mencegah pengeringan permukaan mata. (American Academy of Ophthalmology
Staff, 2011-2012a)
Air mata terdiri dari tiga lapisan, yaitu lipid, aqueous, dan musin. Lapisan
air mata memiliki ketebalan sekitar 8-9 µm. Lapisan lipid memiliki ketebalan 0,1-
0,2 µm dan merupakan lapisan yang terletak paling luar yang berfungsi mencegah
penguapan air mata dan mempertahankan stabilitas air mata. Lapisan aqueous di
bagian tengah memiliki ketebalan 7-8 µm merupakan komponen utama lapisan air
mata. Lapisan aqueous mengandung elektrolit, air, dan protein yang dihasilkan oleh
kelenjar lakrimal utama yang terletak dalam orbita maupun oleh kelenjar lakrimal
tambahan seperti kelenjar Krause dan Wolfring pada konjungtiva. Protein pada
lapisan aqueous meliputi immunoglobulin A (IgA), IgG, IgD dan IgE yang berperan
sebagai mekanisme pertahanan lokal di bagian permukaan mata. Lapisan aqueous

9
selain sebagai antibakteri dan antiviral, juga berfungsi sebagai pelarut nutrisi,
penyedia oksigen, dan menjaga regularitas kornea. Bagian posterior lapisan air
mata adalah lapisan musin dengan ketebalan 1µm mengandung glikoprotein.
Lapisan musin berperan sebagai barrier dari perlengketan maupun penetrasi partikel
asing atau bakteri ke permukaan bola mata. Lapisan musin ini diproduksi oleh
kelenjar goblet konjungtiva. (American Academy of Ophthalmology Staff, 2011-
2012a; American Academy of Ophthalmology Staff, 2011-2012b)
2.1.2 Kelenjar Meibom
Sebuah kelenjar meibom dibentuk oleh sekumpulan secretory acini yang tersusun
sirkular mengelilingi sebuah duktus yang panjang dan secretory acini ini terhubung
dengan duktulus yang lebih pendek. Orifisium dari duktus kelenjar berakhir di batas
posterior palpebra sebelah anterior dari MCJ di tepi palpebra, tempat lipid
disekresikan ke dalam meniscus air mata. (Knop et al., 2011). Kelenjar meibom
terletak di tarsus palpebra berjumlah 30-40 kelenjar di palpebra superior dan 20-30
kelenjar di palpebra inferior. Panjang satu kelenjar dilaporkan sekitar 5,5 mm di
bagian tengah palpebra superior dan 2 mm di palpebra inferior. Kelenjar di palpebra
inferior cederung lebih lebar dari pada di superior. Jumlah secretory acini pada
setiap kelenjar meibom diperkirakan sekitar 10-15 buah dan lebih banyak pada
palpebra superior dibandingkan inferior. (American Academy of Ophthalmology
Staff, 2011-2012a; Knop et al., 2011).
Lipid kelenjar meibom diproduksi di reticulum endoplasma sel meibocyte.
Lipid droplet hasil dari reticumlum endoplasma ini berintegrasi dengan protein dan
asam nukleat membentuk produk sekresi minyak yang disebut dengan meibum.

10
Meibum kemudian disekresikan dari acinus ke sistem duktus dan diteruskan ke tepi
palpebra. Mekanisme pengeluaran sekresi meibum melalui mekanisme tekanan
yaitu (1) melalui sekresi terus menerus oleh secretory acini yang menghasilkan
tekanan di acinus yang menekan meibum ke sistem duktus dan kemudian menuju
orifisium, (2) mekanisme penekanan oleh m. orbicularis oculi yang terletak di luar
tarsus dan m. riolan yang terletak melingkar di bagian terminal kelenjar meibom
pada saat mengedip. (Knop et al., 2011)
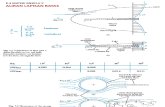
Gambar 2.1 Morfologi kelenjar meibom dan mekanisme pengeluaran
sekresi meibum ke tepi palpebra. (Knop et al., 2011)
2.1.3 Lapisan lipid air mata
Meibum normal memiliki karakteristik berwarna jernih dan cairan lemaknya
dengan mudah menyebar melapisi permukaan mata membentuk lapisan lipid air
mata. Lapisan lipid air mata memiliki ketebalan antara 20 sampai 160 nm yang
terdiri atas dua lapisan yaitu lapisan luar berupa lapisan lipid non-polar dan lapisan

11
dalam berupa lapisan lipid polar (Gambar 2.2). Lipid hasil sekresi kelejar meibom
merupakan campuran kompleks yang mengandung ester kolesterol, triasilgliserol,
kolesterol bebas, asam lemak bebas, fosfolipid, wax esters, dan diesters. Meibum
ini memiliki titik leleh antara suhu 19°C sampai 37°C sehingga pada suhu tubuh
normal 37°C akan dengan mudah untuk keluar ke tepi palpebra (Green-Church et
al., 2011; Macsai, 2008)
Gambar 2.2 Lapisan air mata manusia (Nichols et al., 2011)
Lapisan lipid air mata memiliki fungsi untuk menghambat penguapan,
berperan pada pembiasan cahaya karena posisi pada antarmuka udara-film air mata,
mempertahankan barier hidrofobik yang mencegah air mata mengalir berlebihan
dengan meningkatkan tegangan permukaan. (American Academy of
Ophthalmology Staff, 2011-2012a; Green-Church et al., 2011)
Lapisan lipid air mata berperan penting dalam stabilitas lapisan air mata.
Ketidakstbilan lapisan air mata merupakan salah satu dari mekanisme terjadinya
mata kering terjadi akibat tidak adekuatnya lapisan lipid air mata. Waktu pecah atau

12
break up time air mata dianggap menunjukkan stabilitas air mata. Break up time
merupakan pemeriksaan untuk mengukur kekeringan kornea sesudah satu kedipan
pada waktu tertentu. Pemeriksaan fluoresceine break up time (FBUT) mengukur
waktu yang diperlukan untuk air mata pecah di dalam mata. Uji FBUT berperan
dalam menilai fungsi kelenjar meibom dan dianggap relevan dipakai pada diagnosis
DKM (Tomlinson et al., 2011).
2.2 Disfungsi Kelenjar Meibom
2.2.1 Definisi dan Klasifikasi
Disfungsi kelenjar meibom atau meibomian gland dysfunction (MGD) adalah suatu
abnormalitas kronis dan difus pada kelenjar meibom yang umumnya ditandai
dengan obstruksi duktus terminus dan atau perubahan kuantitatif / kualitatif pada
sekretnya sehingga dapat mengakibatkan perubahan film air mata, gejala-gejala
iritasi mata, inflamasi yang tampak secara klinis dan adanya penyakit permukaan
mata (Nelson et al., 2011).
Terminologi yang digunakan disini adalah disfungsi yang berarti terdapat
gangguan dari fungsi kelenjar meibom. Kelainan pada DKM bersifat difus oleh
karena mengenai sebagian besar kelenjar meibom dan menyebabkan terjadinya
abnormaitas film air mata atau epitel permukaan mata. Aspek yang paling menonjol
pada DKM ini adalah adanya perubahan secara kuantitatif maupun kualitatif dari
sekresi kelenjar meibom. Gejala subjektif berupa iritasi pada mata dimasukkan pada
definisi DKM karena gejala-gejala tersebut paling dirasakan oleh pasien dan
menjadi perhatian utama dokter (Nichols et al., 2011).

13
Gambar 2.3 Klasifikasi DKM oleh International Workshop on MGD dibedakan
menjadi subgrup berdasarkan tingkat sekresi dan kemudian dibagi menjadi
manifestasinya. (Nelson et al., 2011)
Disfungsi kelenjar meibom diklasifikasikan menjadi dua kategori mayor
berdasarkan sekresi kelejar meibom yaitu DKM beraliran kecil (low delivery MGD)
dan DKM beraliran besar (High delivery MGD). DKM beraliran kecil terbagi
menjadi DKM hiposekresi dan DKM obstruktif. DKM obstruktif sendiri terdiri dari
dua subkategori yaitu DKM sikatrik dan non sikatrik. Secara histologi pada DKM
obstruksi terjadi hipertrofi sel epitel duktus dan hiperkeratinasi epitel orifisium.
Hiposekresi kelenjar meibom ditandai dengan penurunan sekresi lipid meibom
tanpa adanya obstruksi. Karakteristik DKM hiperekresi ditandai dengan pelepasan
lipid meibom dalam jumlah besar di tepi palpebra sebagai respon dari adanya
tekanan pada tarsus. Kelainan hipersekresi ini tidak berhubungan dengan adanya

14
peradangan aktif dan tidak adanya perubahan pada struktur kelenjar. (Nelson et al.,
2011)
2.2.2 Epidemiologi dan Faktor Risiko
Prevalensi DKM berkisar antara 3,5 -70 %, angka lebih besar terutama di Asia.
(Schaumberg et al., 2011) Berdasarkan penelitian di Bangkok prevalensi DKM
dilaporkan sebesar 46,2% (Lekhanont et al., 2006), di Shihpai Eye study dilaporkan
sebesar 60,8% (Lin et al., 2003), di Jepang sebesar 61,9% (Uchino et al., 2006) dan
di Beijing sebesar 69,3% (Jie et al., 2009). Prevalensi di Asia ini sangat berbeda
dengan di populasi kaukasia yaitu 3,5% pada penelitian Salisbury dan 19,9% di
Australia. (Schaumberg et al., 2011) Disfungsi kelenjar meibom merupakan
gangguan yang umum ditemukan pada praktek dokter mata. Hom et al (1990)
melaporkan prevalensi DKM sebesar 38,9 % sedangkan Morniali dan Stanek
(2000) menemukan prevalensi sebesar 33% pada pasien berusia kurang dari 30
tahun dan 71,1% pada individu berusia 60 tahun atau lebih. (Matsumoto et al.,
2008; Hom et al., 1990; Morniali and Stanek, 2000)
Faktor lokal mata, sistemik dan pengobatan berperan pada perkembangan
DKM. Faktor lokal di mata yang berperan termasuk blefaritis, penggunaan lensa
kontak, dan penyakit mata kering. Kelainan sistemik yang berperan dalam DKM
antara lain defisiensi androgen, menopause, penuaan, sindrom Sjogren, kadar
kolesterol darah, psoriasis, rosacea, hipertensi, dan hiperplasia prostat jinak. Faktor
medikasi juga dihubungkan dengan patogenesis DKM yaitu antiandrogen,
pengobatan untuk mengobati BPH, terapi hormon pascamenoupause seperti
estrogen dan progestin, antihistamin, antidepresan dan pemakaian retinoid.

15
Sedangkan konsumsi asam lemak omega-3 merupakan faktor protektif. (Nichols et
al., 2011)
2.2.3 Patogenesis Disfungsi Kelenjar Meibom
Knop et al. (2011) menggambarkan faktor-faktor yang berperan dalam patogenesis
DKM. Faktor penyebab yang sudah diketahui yaitu proses penuaan, umur, jenis
kelamin, gangguan hormon, faktor lingkungan, lensa kontak, dan perubahan
kualitas atau kuantitas meibum saling berinteraksi menyebabkan terjadinya
hiperkeratinisasi sistem duktus kelenjar meibom, peningkatan viskositas meibum,
atrofi acinar kelenjar. (Knop et al., 2011)
Hiperkeratinisasi dan peningkatan viskositas meibum merupakan
mekanisme inti dalam terbentuknya obstruksi orifisium kelenjar meibom yang akan
menyebabkan pengeluaran meibum ke tepi palpebra sangat rendah. Obstruksi
orifisium ini juga menyebabkan stasisnya meibum di sistem duktus menyebabkan
peningkatan tekanan, dilatasi sistem duktus dilanjutkan terjadinya atrofi acinar
yang akhirnya menyebabkan sekresi meibum rendah. (Knop et al., 2011)
Perubahan pada kualitas dan kuantitas meibum mengakibatkan terjadinya
penurunan viskositas dan atau peningkatan volume sekresi meibum. Adanya
perubahan viskositas, volume sekresi dan stasisnya meibum oleh karena obstruksi
menyebabkan bakteri-bakteri permukaan mata semakin berkembang. Bakteri
komensal seperti stafilokokus koagulase negative, Staphylococcus aureus, dan
Propionibacterium acnes dihubungkan dan berkontribusi terhadap patogenesis
DKM. Bakteri yang tumbuh di permukaan mata tersebut melepaskan enzim lipase
yang memicu pelepaskan mediator-mediator toksik seperti asam lemak dan

16
menginisiasi reaksi peradangan subklinis dengan dilepasakan sitokin peradangan.
Mediator-mediator toksik ini akhirnya akan memicu terjadinya penyakit mata
kering tipe evaporative. (Knop et al., 2011)
Gambar 2.4 Skema patogenesis DKM (Knop et al., 2011)
2.2.4 Diagnosis Disfungsi Kelenjar Meibom
Penegakan diagnosis DKM berdasarkan anamnesis, pemeriksaan oftalmologi dan
pemeriksaan penunjang. Keluhan yang timbul pada DKM meliputi rasa terbakar,
sensasi benda asing, hiperemia palpebra dan konjungtiva, dan kalazian rekuren.
Penggunaan kuisener Seperti Ocular Surface Disease Index (OSDI) dapat
digunakan untuk mengetahui secara lengkap keluhan-keluhan mata kering yang
muncul akibat DKM (American Academy of Ophthalmology Staff, 2011-2012b,
Tomlinson et al., 2011).

17
Tanda klinis DKM ditemukan adanya dropout kelenjar meibom, perubahan
sekresi kelenjar, dan perubahan morfologi palpebral. Dropout kelejar meibom
mengacu pada hilangnya jaringan acinar yang terditeksi melalui pemeriksaam
meibografi. Dropout kelenjar meibom meningkat seiring dengan bertambahnya usia
pada subjek normal. Jumlah kelenjar yang dropout dapat menunjukan keparahan
dari DKM. Kehilangan dapat terjadi di bagian proximal, centra, distal atau
keseluruhan kelenjar. Dropout kelenjar yang ekstensif dihubungkan dengan
peningkatan penguapan air dari mata. (Tomlinson et al., 2011)
Perubahan sekresi kelenjar meibom dinilai dari kualitas dan expresibilitas
meibum. Untuk mengetahui expresibilitas kelenjar meibom dilakukan penekanan
dengan jari tangan pada palpebra. Pada subjek normal penekanan yang ringan sudah
mampu mengeluarkan sekresi kelenjar meibom, sedangkan penekanan yang lebih
keras dilakukan pada derajat meibum yang lebih tebal. Ekspresibilitas kelenjar
meibom dinilai menggunakan skala 0 -3 dilihat pada 8 kelenjar meibom di palpebra
inferior atau superior. Berdasarkan jumlah kelenjar yang mengeluarkan sekresi /
ekspresibilitas : skor 0 (bila semua kelenjar); skor 1, (3 sampai 4 kelenjar); skor 2,
(1 sampai 2 kelenjar), dan nilai skor 3 (bila tidak ada kenjar sama sekali). Pada
DKM kualitas dari minyak yang terekspresi bervariasi antara cairan keruh, cairan
viscous yang mengandung partikulat dan berwarna keruh tebal, dan material seperti
pasta gigi. Skor yang digunakan menggunakan sistem 4 nilai yaitu skor 0 (jernih
/normal); skor 1 (keruh) ; skor 2 (keruh dengan partikel); skor 3 (seperti pasta gigi).
Kualitas sekresi ini dinilai pada 8 kelenjar di palpebral superior dan inferior. Skor
kelenjar meibom didapatkan dengan menjumlahkan skor ekspresibilitas dan skor

18
0 1
2 3
kualitas sekresi. Menurut IWMGD bila umur <= 20 tahun nilai 1 pada skor
ekspresibiltas atau kualitas sekresi dianggap abnormal, bila umur <= 20 tahun nilai
skor 1 pada skor ekspresibiltas dan kualitas sekresi dianggap abnormal, atau nilai >
1 pada salah satu skor eksresibilitas atau kualitas sekresi meibom (American
Academy of Ophthalmology Staff, 2011-2012b; Tomlinson et al., 2011)
Gambar 2.5 Derajat Disfungsi Kelenjar Meibom (Abelson and Oberoi, 2006;
Tomlinson et al., 2011; Bron, Benjamin and Snibson, 1991)
Penelitian oleh Paiva et al. (2003) yang membandingkan normal subjek
dengan subjek yang mengeluh iritasi mata didapatkan perubahan mofologi palpebra
dapat dilihat adanya metaplasia di orifisium kelenjar, brush mark (tanda vascular
linear). Perubahan morfologi palpebral oleh Arita et al. (2009) dinilai dari ada atau
tidak abnormalitas palpbera seperti : irregularitas palpebra, engorgement pembuuh
darah palpebra, penyumbatan orifisium kelenjar meibom dan pergeseran anterior

19
atau posterior dari pertautan mukokutaneous. (Tomlinson et al., 2011; Arita et al.,
2009; Paiva et al., 2003)
Pemeriksan penunjang lain dilakukan selain untuk diagnosis DKM itu
sendiri juga dilakukan terutama untuk mengetahui apakah ada penyakit yang
berhubungan dengan DKM. Pemeriksaan lain yang dilakukan yaitu pemerikaan
untuk mengetahui kualitas dan kuatitias lapisan air mata seperti pemeriksaan
lapisan lipid air mata, tes penguapan, osmolaritas, stabilitas, volume dan sekresi
serta pemeriksaan tanda peradangan pada pemukaan mata (Tomlinson et al., 2011).
Pemeriksaan FBUT adalah Pemeriksaan untuk mengetahui stabilitas lapisan air
mata. Tes ini dikerjakan dengan menggunakan floresin yang diteteskan di fornix
konjungtiva, kemudian subjek diperintahkan untuk berkedip beberapa kali.
Pemeriksaan dilakukan di slit lamp dengan filter biru, subjek diminta berkedip
secara alami dan setelah kedipan terakhir dimulai pengukuran waktu pecahnya film
air mata atau bintik hitam di kornea. Nilai FBUT normal adalah >10 detik.
Sensitifitas dan spesifitas pemeriksaan FBUT dilaporkan sebesar 72% dan 62%.
(Tomlinson, et al., 2011). Pemeriksaan Schirmer I adalah pemeriksaan untuk
mengetahui kualitas sekresi air mata. Tes ini dikerjakan dengan menggunakan
kertas filter Schirmer pada sepetiga lateral kelopak mata bawah selama 5 menit
dengan mata terpejam. Pemeriksaan dilakukan tanpa pemeberian anestesi topical.
Panjang kertas filter yang basah karena air mata dinyatakan dalam millimeter
(American Academy of Ophthalmology Staff, 2011-2012b).

20
2.2.5 Penatalaksanaan Disfungsi Kelenjar Meibom
Penatalaksanaa DKM disesuaikan dengan derajat keparahan DKM. IWMGD
merekomendasikan algoritma penatalaksanaan DKM berdasarkan pendekatan
berbasis bukti. (Nichols et al., 2011) Algoritma disusun berdasarkan keluhahan,
tanda klinis DKM yaitu kualitas sekresi meibum, ekspresibilitas, dan morfologi tepi
palpebra serta perwarnaan permukaan mata (Tabel 2.1).
Tabel 2.1 Algoritma penalaksanaan DKM berdasarkan pendekatan bukti (Nichols
et al., 2011)
Derajat Tanda Klinis Penalaksanaan
1 Tidak ada keluhan mata tidak
nyaman, gatal atau silau
Tanda Klinis DKM berdasarkan
ekspresi kelenjar meibom
- Perubahan Sekresi minimal
: Gradasi ≥2-4
- Ekspresibilitas : 1
Tanpa pewarnaan permukaan mata
Informasi kepada pasien tentang
DKM, akibat potensial dari diet,
dan efek lingkungan rumah atau
tempat kerja terhadap air mata.
Pertimbangan higienitas
palpebra termasuk penghangatan
dan penekanan
2 Keluhan minimal sampai ringan
dari keluhan tidak nyaman mata,
gatal, atau silau
Tanda klinis DKM minimal sampai
ringan
- Fitur tepi palpebra yang
tersebar
- Perubahan sekresi ringan :
gradasi ≥4 - <8
- Ekspresibilitas : 1
Pewarnaan permukaan mata
terbatas
Saran pada meningkatkan
kelembaban, optimalisai tempat
kerja dan peningkatan konsumsi
asam lemak omega-3
Higienitas palpebra dengan
penghangatan ( minimal 4 menit,
1 – 2 kali sehari) diikuti dengan
pemijatan dan pengeluaran
sekresi kelenjar
Semua yang disebutkan diatas
dikombinasi :
- Air mata buatan
- Azitromicin topikal
- Spray liposomal
- Pertimbangkan derivat
tetrasiklin oral

21
3 Keluhan sedang pada rasa tidak
nyaman, gatal, dan silau
Tanda klinis DKM sedang
- Fitur tepi palpebra :
penyumbatan, vaskularitas
- Perubahan sekresi sedang :
gradasi ≥8 - <13
- Ekspresibilitas : 2
Perwarnaan konjuntiva dan kornea
perifer, lebih sering di inferior
ringan sampai sedang
Terapi seperti yang disebutkan
pada stage 2 plus:
- Derivat tetrasiklin oral
- Salep lubrikasi saat tidur
- Terapi anti peradangan
untuk mata kering sesuai
indikasi
4 Keluhan yang jelas pada rasa tidak
nyaman pad amata , gatal dan silau
yang mengganggu aktivitas sehari-
hari
Tanda klinis DKM berat
- Fitur tepi palpebra :
droupout, displacement
- Perubahan sekresi sedang :
gradasi ≥13
- Ekspresibilitas : 3
Peningkatan perwarnaan
konjungtiva dan kornea termasuk
pewarnaan sentral
Peningktan tanda peradangan :
hiperemi konjungtiva
Terapi seperti yang disebutkan
pada stage 3 , plus
- Terapi anti peradangan
untuk mata kering
Suplementasi asam lemak omega-3 mendapatkan kenaikan popularitas
dalam beberapa tahun terakhir karena efek anti peradangan. Asam lemak omega-3
dan omega-6 menurunkan ekspresi tanda peradangan konjungtiva HLA-DR dan
mungkin membantu memperbaiki keluhan mata kering (Brignole-Baudouin et al.,
2011). Terdapat hubungan antara komsumsi asam lemak omega-3 per oral dengan
penurunan laju penguapan air mata, perbaikan pada keluhan mata kering dan
peningkatan sekresi air mata (Kangari et al., 2013). Hal yang sama juga ditemukan
oleh Bhargava et al. (2013) bahwa terdapat perbedaan yang signifikan pada

22
peningkatan nilai test Schirmer, FBUT dan penurunan keluhan pada kelompok
omega-3 dibandingkan kontrol. (Kangari et al., 2013; Bhagava et al., 2013;
Brignole-Baudouin et al., 2011)
Efikasi suplementasi asam lemak omega-3 pada DKM telah dilaporkan pada
berbagai penelitian. Pinna et al (2007) melaporkan superioritas suplementasi
omega-3 dibandingkan dengan placebo atau higienitas palpebra pada pasien dengan
DKM. Macsai (2008) melaporkan penelitian randomize clinical trial untuk menilai
efikasi omega-3 pada pasien dengan DKM obstruksi ringan dan blefaritis yang telah
mendapatkan terapi topical dan tetrasiklin oral. Pada penelitian tersebut didapatkan
perbaikan pada keluhan dan tanda objektif seperti stabilitas dan produksi air mata,
pewarnaan permukaan mata, asesmen kelenjar meibom, evaluasi meibum antara
baseline dengan setelah 1 tahun pengukuran. Untuk pengukuran FBUT, Meibum
skor, OSDI tidak ditemukan perbedaan antara kedua grup perlakuan dan placebo
karena kedua grup memberikan perbaikan. Penelitian lain oleh Olenik didapatkan
hasil yang sama yaitu terjadi perbaikan OSDI, FBUT, peradangan tepi kelopak
mata, dan sekresi kelenjar meibom setelah pemeberian kapsul omega-3 selama 3
bulan. (Macsai, 2008; Olenik et al., 2013; Pinna et al., 2007)
2.3 Dislipidemia
Dislipidemia adalah keadaan yang ditandai oleh abnormalitas kadar lipid darah
yaitu peningkatan kadar trigliserida, LDL, kolesterol total dan penurunan kolesterol
HDL. Dislipidemia menurut ATP III adalah Total kolesterol (TC) > 200 mg/dl, TG
> 150 mg/dl , LDL > 130 mg/dl, HDL <40 mg/dl. (Adult Treatment Panel III, 2002)

23
Tabel 2.2 Kadar lipid serum normal menurut NCEP (National Cholesterol
Education Program) ATP III (Adult Treatment Panel III) (2000) (dalam mg/dl)
Total Kolesterol
<200
200-239
≥240
Optimal
Diinginkan
Tinggi
LDL
<100
100-129
130-159
160-189
≥190
Optimal
Mendekati optimal
Diinginkan
Tinggi
Sangat tinggi
Trigliserida
<150
150-199
200-499
≥500
Optimal
Diinginkan
Tinggi
Sangat tinggi
HDL
<40
≥60
Rendah
Tinggi
Penelitian-penelitian mengenai lipid yang sudah dilakukan sebagian besar
diutamakan pada risiko penyakit kardiovaskular dan serebrovaskular. Dislipidemia
merupakan faktor risiko terjadinya penyakit jantung koroner. Keadaan
hiperkolesterolemia menginduksi terjadinya proses atherogenesis yang memicu
pembentukan antherosklerosis pada pembuluh darah. Penelitian epidemiologi
menunjukkan bahwa peningkatan kadar LDL dan penurunan kadar HDL dengan
atau tanpa faktor risiko lain meningkatkan risiko kejadian kardiovaskular. (Wilson
et al., 1998)
Prevalensi disipidemia di Amerika serikat didapatkan kadar kolesterol total
lebih dari 200 mg/dl adalah sebesar 45,% dan kolesterol total lebih dari 240mg/dl
adalah sebesar 15,7%. Sedangkan prevanlensi LDL > 130 mg/dl 32,8%, HDL <40
mg/dl 15,5% dan trigliserida > 150 mg/dl adalah 33,1%. (Dao et al., 2010) Di

24
Indonesia prevalensi dislipidemia semakin meningkat. Survei MONICA III tahun
2000 dengan responden sebanyak 1856 yang terdiri dari 60,3% wanita dan 39,7%
laki-laki didapatkan profil lipid plasma menunjukkan kadar kolesterol total rata-rata
209,96 ± 45,47 mg/dl, HDL rata-rata 42,89 ± 11,66 mg/dl, sedangan LDL 141,11
± 37,65 mg/dl, dan trigliserida 130,30 ± 81,89 mg/dl. Proporsinya ditemukan
hiperkolesterolemia > 250 mg/dl sebanyak 27.7%, 200mg/dl sebanyak 56.5%, HDL
< 40mg/dl sebanyak 47.3%, LDL > 160 sebanyak 28.8%, trigliserida > 160
sebanyak 22.0% dan rasio kolesterol total/HDL > 5 sebanyak 51.9%. (Supari, 2007)
Penatalaksaan dislipidemia terdiri atas nonfarmakologis dan penggunaan
obat penurun lipid. Penatalaksanaan nonfarmakologi disarankan untuk dilakukan
terlebih dahulu kemudian dilanjutkan dengan pemberian obat penurun lipid.
Perubahan gaya hidup merupakan penatalaksanaan non-farmakologi yang meliputi
terapi nutrisi medis dan aktivitas fisik. Omega-3 merupakan salah satu obat untuk
menurunkan kadar kolesterol darah. (Adam, 2009)
2.4 Disfungsi Kelenjar Meibom dan Dislipidemia
Hubungan antara kejadian dislipidemia dan DKM masih menjadi kontrovesi. Dao
et al (2010) menemukan bahwa pasien dengan DKM derajat sedang sampai berat
diketahui insiden dislipidemia lebih tinggi pada peningkatan kadar total kolesterol
> 200mg/dlibandingkan kontrol. Namun pada penelitian tersebut tidak terdapat
perbedaan yang signifikan pada kadar LDL, HDL dan trigliserida. (Dao et al., 2010)
Penelitian lain oleh Pinna et al., (2013) menemukan terdapat perbedaan
kadar kolesterol total, LDL dan HDL pada pasien DKM tanpa riwayat
hiperkolesterolemia sebelumnya dibandingkan dengan kontrol. Penelitian ini juga

25
menemukan kejadian hiperkolesterolemia >200 mg/dl sebesar 58% pada pasien
DKM. (Pinna et al., 2013)
Hasil berbeda didapatkan oleh Bukhari et al. (2013) bahwa tidak ada
korelasi antara DKM dengan dislipidemia. Penelitian ini ternyata menemukan
bahwa prevalensi tingginya kadar triglierida dan LDL meningkat sesuai dengan
meningkatnya derajat DKM. Prevalensi meningkatnya kadar trigliserida pada DKM
derajat 1 5,7%, derajat 2 14,6%, 39,3% pada derajat 3. Kadar LDL tinggi
didapatkan pada derajat 1 sebesar 17,1%, derajat 2 29,3% dan derajat 3 35,7%. Hal
ini terjadi karena skresi kelenjar meibom yang mengandung trigliserida sebesar 1%-
2% pada sekresi meibum normal. Peningkatan kadar trigliserida dan LDL
kemungkinan memberi peran pada peningkatan titik leleh meibum dan penurunan
viskositasnya yang pada akhirnya menyebabkan buntunya orifisium kelenjar
meibom. (Bukhari, 2013)
2.5 Asam Lemak Omega-3
Terdapat 2 jenis Polyunsuturated Fatty Acid (PUFA) yaitu omega-3 dan omega-6.
Omega-3 dan omega-6 merupakan lemak esensial yang diperlukan pada proses
pertumbuhan dan perkembangan. Asam lemak omega-3 terdiri atas 2 subkelas pada
dalam diet manusia yang bersumber dari tumbuhan dan makanan laut. Subkelas
pertama yang lebih dahulu diketahui terdiri dari 1 asam lemak omega-3 yaitu α-
linolenic acid (ALA) dan subkelas kedua terdiri dari 3 asam lemak omega-3 yaitu
eicosapentaenoic acid (EPA), docosapentaenoic acid (DPA) dan docosahexaenoic
acid (DHA). (Macsai, 2008; Harris and Jacobson, 2009)

26
Omega-3 dan omega-6 bersaing untuk enzim yang sama untuk akhirnya
akan dikonversi menjadi prostaglandin anti inflamasi (PGE3) dan leukotrin
inflamasi rendah pada omega-3 dan omega-6 dikonversi mejadi prostaglandin pro
inflamasi (PGE2) dan leukotrin dengan inflamasi lebih banyak. Calder (2003)
mendemontrasikan bahwa produksi berlebihan dari PGE2 dan produksi yang
rendah dari PGE1 dan PGE3 yang bersifat anti infalmasi terjadi pada perbandingan
omega-6 dan omega-3 yang tinggi. (Macsai, 2008; Calder, 2003)
Omega-3 memodulasi metabolism prostaglandin melalui sintesis PGE3
sebagai inhibitor kompetitif pada jalur asam arakidonat. Pada fase awal terjadinya
inflamasi, sejumlah besar interleukin dan mediator lipid dilepaskan. Eicosanoid
proinflamasi dari metabolism arakidonat dilepaskan dari membrane fosfolipid di
tempat inflamasi diaktifkan. Eicosapentaenoic acid berkompetisi dengan asam
arakidonat untuk sintesis prostaglansin dan leukotriene antiinflamasi oleh EPA dan
proinflamasi oleh asam arakidonat pada tingkat siklooksigenasi dan lipooksigenasi.
(Macsai, 2008)
Peningkatan jumlah EPA dan DHA sistemik menyebabkan : (1). Penurunan
produksi prostaglandin E2, (2). Penurunan thromboxane A2, platelet aggregator
dan vasokonstritor poten, (3). Penurunan pembentukan leukotriene B4, pemicu
inflamasi, kemotaksis leukosit dan aderen, (4). Peningktan thromboxane A3,
platelet aggregator dan vasokontriktor lemah, (5) peningkatan prostacyclin PGI3,
inhibitor agregasi platelet (6). Peningkatan leukotriene B5 , pemicu inflai dan agen
kemotaksis yang lemah. (Macsai, 2008)

27
Gambar 2.6 Jalur metabolik omega-3 dan omega-6 (Macsai, 2008)
2.5.1 Mekanisme Kerja Omega-3 pada Disfungsi Kelenjar Meibom
Salah satu penyebab terjadinya DKM adalah adanya hiperkeratinasi dan
pathogenesis lain yang berhubungan seperti dilatasi duktus dan atrofi acinar.
Penyebab lain seperti atopi, pempigoid, acne rosasea, dan seboroic dihubungan
dengan DKM dan inflamasi kronis di permukaan mata. Salah satu mekanisme kerja
omega-3 pada penyakit mata kering dan DKM adalah efek dari pemecahan omega-
3 menghasilkan molekul yang mampu menekan inflamasi. Metabolime omega-3
menyebabkan penghambatan metabolism omega-6 yang bersifat proinflamasi yang
kemudian menurunkan status inflamasi di tepi palpebra dan daerah sekitar kelenjar
meibom. Pada pasien dengan DKM dan penyakit mata kering yang merupakan

28
akibat dari inflamasi, penurunan status inflamasi sitemik juga meringankan keluhan
mata kering dan DKM (Brignole-Baudouin et al., 2011; Macsai, 2008)
Macsai (2008) melaporkan bahwa pemberian suplementasi omega-3 pada
DKM selain berperan sebagai antiinflamasi juga berperan pada perubahan jenis dan
komposisi asam lemak pada sekresi kelenjar meibom. Hal tersebut bermanfaat
kepada stabilitas lapisan air mata dan kemungkinan mencegah stagnasi dan
inflamasi di duktus kelenjar meibom. (Macsai, 2008)
2.5.2 Dosis Omega-3 Pada Disfungsi Kelenjar Meibom
Sampai saat ini belum terdapat rekomendasi mengenai dosis omega-3 yang
diberikan pada disfungsi kelenjar meibom. Beberapa penelitian yang sudah
dilakukan pemberian 2 gram sebanyak 3 kali sehari omega-3 dalam bentuk flaxeed
oil memberikan efek penurunan skor meibum secara signifikan (Macsai, 2008).
Dosis 6 gram flaxeed oil diberikan mengacu pada dosis maksimal per hari yang
boleh diberikan.
Penelitian lain oleh Olenik et. al. tahun 2013 didapatkan terjadi perbaikan
pada skor OSDI, FBUT, peradangan tepi kelopak mata, dan ekspresi kelenjar
meibom yang menggunakan kapsul omega-3 1,5 gram per hari selama 3 bulan,
dosis per kapsul mengandung 350 mg DHA, 42,5 mg EPA dan 30 mg DPA. (Olenik
et al., 2013)
2.5.3 Efek samping Omega-3
Efek samping yang bisa terjadi bila mengkonsumsi omega-3 adalah alergi terhadap
omega-3, rasa tida nyaman seperti mual, peningkatan terjadinya perdarahan dan
peningkatan risiko kangker prostat pada laki-laki. Perdarahan terjadi karena omega-

29
3 menghambat fungsi platelet melalui mekanisme kompetisi dengan asam
arakidonat yang berperan pada pembentukan eicosanoid pada siklooksigenase.
(Harris dan Jacobson, 2009). Pasien yang mendapat dosis omega-3 dengan rentang
2-5 gram per hari tidak ditemukan bukti adanya peningkatan tendensi terjadinya
perdarahan. (Macsai, 2008)
Hubungan antara konsumsi omega-3 dengan kejadian kangker prostat masih
menjadi kontroversi. Peningkatan risiko terjadinya kangker prostat diketahui
berdasarkan peningkatan kadar serum prostat spesifik antigen (PSA) pada subjek
yang mendapatkan suplemen omega-3 (Brouwer et al., 2013). Kadar PSA pada
pasien yang mengkonsusi omega-3 didapatkan sebesar 0,52 ng/mL dibandingkan
dengan placebo sebesar 0,42 ng/mL namun secara statistik tidak bermakna
(Brouwer et al., 2013)